Centro de recursos


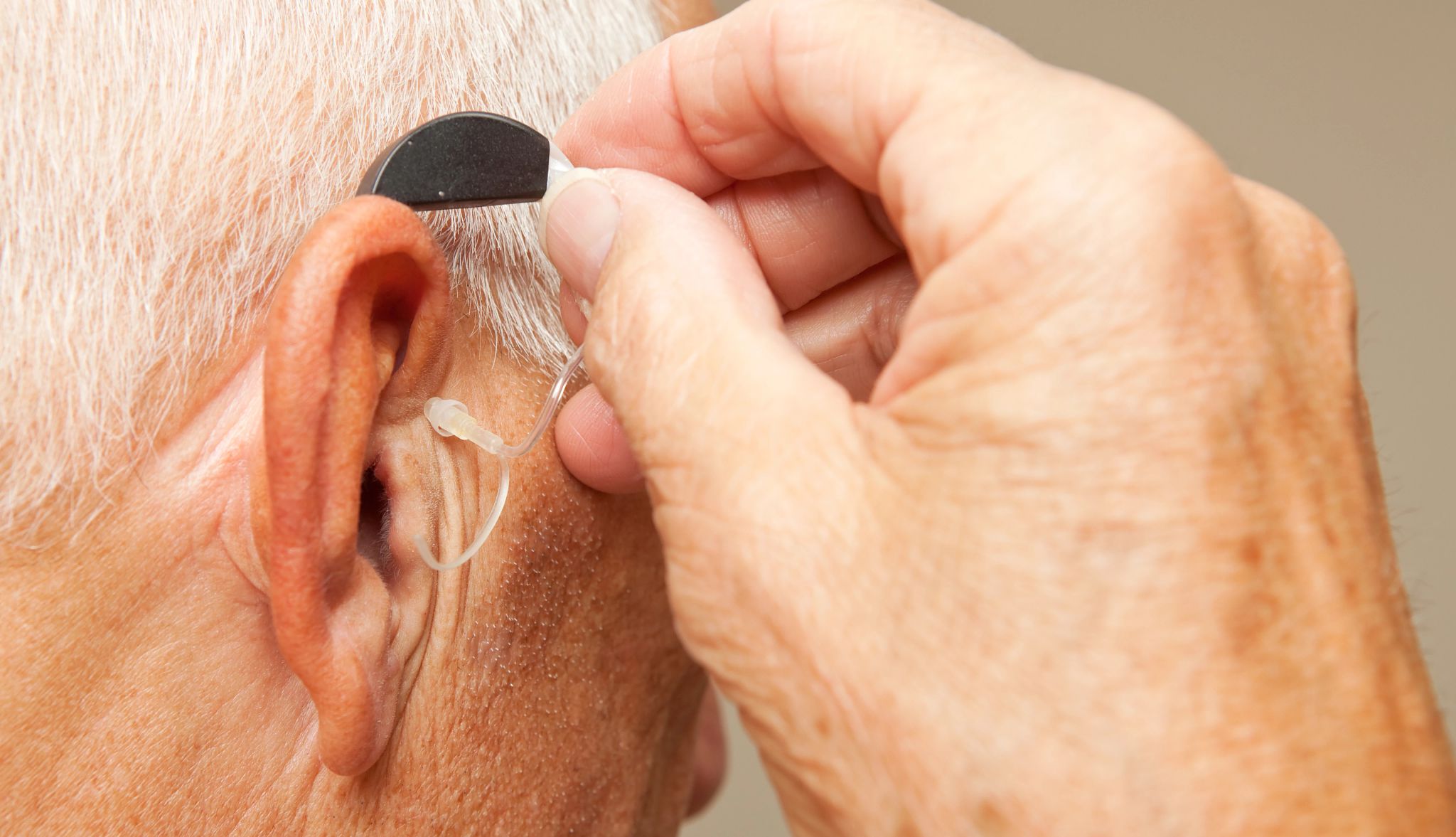
El Departamento de Salud y Servicios Humanos de EE.UU. (HHS) finalizó una norma que permitirá la importación de ciertos medicamentos recetados de Canadá. No obstante, los funcionarios no pudieron predecir la cantidad de dinero que podrían ahorrar los consumidores o la fecha en la que se pondrán en marcha los programas para reducir los costos de los medicamentos.
La normativa prepara el camino para que Florida, Colorado, Maine, Vermont, Nuevo Hampshire y Nuevo México empiecen el proceso de implementar leyes ya aprobadas para permitir la importación de ciertos medicamentos recetados. Los estados deben obtener autorización del HHS para iniciar sus programas.


Membresía de AARP: $15 por tu primer año cuando te inscribes en la renovación automática.
Obtén acceso inmediato a productos exclusivos para socios y cientos de descuentos, una segunda membresía gratis y una suscripción a AARP The Magazine.
Únete a AARP
"Creemos que esta norma propuesta es, potencialmente, un instrumento efectivo para implementar las leyes que ya han aprobado varios estados, las cuales ayudarían a que ciertos medicamentos sean más económicos", comentó David Certner, asesor legislativo y director de Política Legislativa para Asuntos Gubernamentales de AARP, en una carta enviada en marzo (en inglés) al Dr. Stephen Hahn, comisionado de la Administración de Alimentos y Medicamentos (FDA). La carta de Certner, en la que se menciona la norma planteada, insta a la Administración de Trump a formular otras propuestas "para ayudar a reducir los precios de los medicamentos y asegurar el acceso a los fármacos que tanto se necesitan". Además, la carta exhorta firmemente al Gobierno federal a "continuar trabajando con el Congreso para promulgar leyes significativas sobre medicamentos recetados, las cuales ayudarían a reducir los precios y los costos de bolsillo relacionados con los fármacos".



































.jpg?crop=true&anchor=13,195&q=80&color=ffffffff&u=lywnjt&w=2008&h=1154)






























También te puede interesar
La misión de la fundadora de AARP empieza con una visita a un gallinero.
Ethel Percy Andrus encuentra a una maestra retirada viviendo de manera deplorable.Veteranos afroamericanos: una historia de heroísmo
De la Guerra Civil a los conflictos actuales, estos soldados realizaron actos de heroísmo y valor.
AARP hace realidad los sueños
El programa Wish of a Lifetime ha servido a más de 2,000 adultos mayores.