Centro de recursos

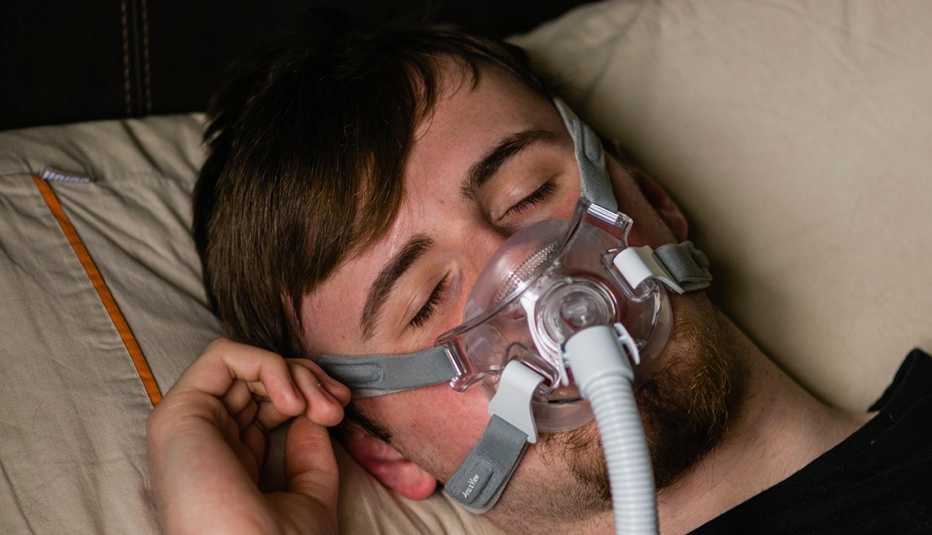
Se emitió un retiro del mercado (en inglés) de 17 millones de mascarillas para la apnea del sueño fabricadas por Philips que contienen clips magnéticos. Según se informa, esos clips han afectado implantes metálicos médicos y objetos en el cuerpo, como marcapasos, desfibriladores cardioversores y neuroestimuladores.
Las mascarillas para la terapia de CPAP y BiPAP (también conocida como PAP de dos niveles) retiradas tienen clips que fijan las correas que sujetan la mascarilla a la cabeza. Sin embargo, las nuevas advertencias dicen que las mascarillas no se deben usar si el paciente, los miembros del hogar, los cuidadores o las personas que duermen en la misma cama tienen un implante médico metálico.


Membresía de AARP: $15 por tu primer año cuando te inscribes en la renovación automática.
Obtén acceso inmediato a productos exclusivos para socios y cientos de descuentos, una segunda membresía gratis y una suscripción a AARP The Magazine.
Únete a AARP
Philips ha recibido 14 informes de pacientes que dijeron que los imanes de la mascarilla pueden haber afectado sus dispositivos médicos y causado problemas como falla de un marcapasos, interrupción de un desfibrilador, cambios en los latidos del corazón y problemas cognitivos. No se ha vinculado ninguna muerte con el retiro del mercado, pero el anuncio (en inglés) dijo que es posible que haya resultados mortales.
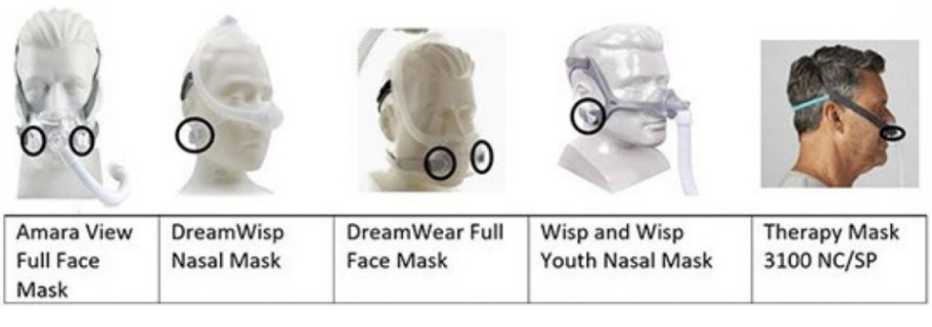
Las mascarillas retiradas del mercado incluyen la Amara View Full Face Mask, la DreamWisp Nasal Mask, la DreamWear Full Face Mask, la Wisp and Wisp Young Nasal Mask y la Therapy Mask 3100 NC/SP.
Este retiro no está relacionado con un anuncio del año pasado sobre máquinas de apnea del sueño de Philips cuya espuma los pacientes corrían el riesgo de inhalar.

Consejos para los consumidores
Las mascarillas retiradas del mercado pueden continuar usándose, siempre y cuando los pacientes y las personas cerca de ellos no tengan implantes metálicos, dijo Philips en sus instrucciones actualizadas y en las etiquetas de los productos.



































.jpg?crop=true&anchor=13,195&q=80&color=ffffffff&u=lywnjt&w=2008&h=1154)






























También te puede interesar
6 señales de advertencia de la apnea del sueño
Esta grave enfermedad tiene algunos efectos sorprendentes en todo, desde la presión arterial hasta la vida sexual.
¿Cuál es la posición más saludable para dormir?
La forma en que duermes puede afectar la calidad del sueño y la salud del cerebro, el corazón y el estómago.
6 causas comunes de los ronquidos (y cuándo preocuparse)
Los ronquidos se producen por problemas de salud que pueden variar de leves a graves.