Vida Sana

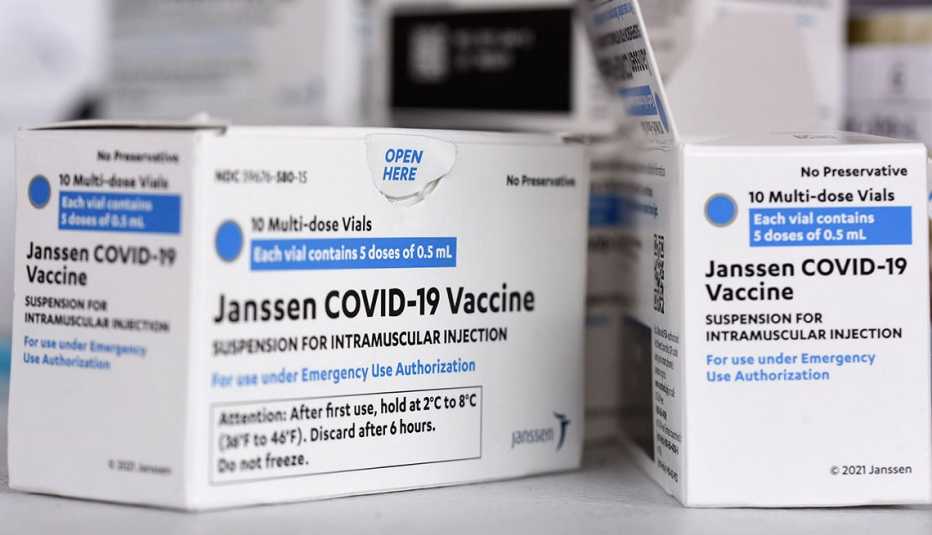
Las personas de 18 años o más que todavía no se han vacunado contra la COVID-19 deberían recibir la vacuna de Johnson & Johnson solo si las vacunas de Pfizer-BioNTech y de Moderna no están disponibles o no son médicamente adecuadas, o si recibir el producto de J&J es la única manera de vacunarse, según mencionaron los reguladores federales el 5 de mayo en una actualización a la autorización para el uso de emergencia de la vacuna.
La razón, señaló en su anuncio (en inglés) la Administración de Alimentos y Medicamentos de EE.UU. (FDA), se debe a una complicación poco común —pero potencialmente mortal— llamada síndrome de trombosis-trombocitopenia (TTS), que se relacionó por primera vez con la vacuna de J&J en la primavera del 2021. Desde entonces, las autoridades de salud han monitoreado e investigado todos los casos de TTS, que se presenta cuando se forman coágulos de sangre y la persona también tiene niveles bajos de plaquetas en la sangre.


Membresía de AARP: $12 por tu primer año cuando te inscribes en la renovación automática.
Obtén acceso inmediato a productos exclusivos para socios y cientos de descuentos, una segunda membresía gratis y una suscripción a AARP The Magazine.
Únete a AARP
Se han reportado alrededor de 3.23 casos de TTS por cada millón de dosis de J&J; algunos han sido mortales. Las personas que se administraron la vacuna de J&J hace meses no deberían preocuparse, ya que los síntomas del síndrome por lo general aparecen entre una y dos semanas después de la inoculación. La mayoría de los casos se han presentado en mujeres, generalmente menores de 50 años, y las tasas más altas se han registrado entre las mujeres de 30 a 49 años. Según datos (en inglés) de los Centros para el Control y la Prevención de Enfermedades (CDC), se han reportado muy pocos casos de TTS en personas de 65 años o más. Las vacunas de Pfizer y Moderna se fabrican utilizando la tecnología ARNm, que es diferente a la que utiliza el producto de J&J.
El TTS es una complicación poco común pero continua
Cuando los casos de TTS aparecieron por primera vez la primavera pasada, las autoridades de salud suspendieron el uso de la vacuna de J&J para estudiar su seguridad, y con el tiempo determinaron que sus beneficios superaban cualquier riesgo.

































































También te puede interesar
Mutaciones de ómicron: lo que debes saber sobre las últimas subvariantes
BA.2, BA.2.12.1 y otras cepas que circulan caen bajo la categoría de ómicron.4 maneras en que las mascarillas pueden fomentar la salud
¿Alergias? ¿Asma? Tu mascarilla puede añadir otra capa de protección.
7 tipos de medicamentos que pueden dañar tus dientes
Docenas de medicamentos comunes pueden afectar la boca, las encías y causar otros problemas de salud dental.